- MyoD
-
Proteína 1 de diferenciación miogénica 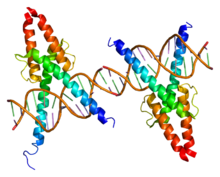
Estructura tridimensional de la proteína MyoD.HUGO 7611 Símbolo MyoD Símbolos alt. PUM; MYF3; MYOD1 Datos genéticos Locus Cr. 11 p15.1 Bases de datos Entrez 4654 OMIM 159970 PDB 1mdy RefSeq NP_002469 UniProt P15172 La proteína 1 de diferenciación miogénica (MyoD) es una proteína humana con un importante papel en la regulación de la diferenciación del tejido muscular. MyoD pertenece a una familia de proteínas conocidas como factores reguladores miogénicos (MRFs).[1] Son factores de transcripción con dominios hélice-bucle-hélice básicos que actúan secuencialmente en el proceso de diferenciación miogénica. Entre los miembros de la familia MRF cabe destacar MyoD, Myf5, miogenina y MRF4 (Myf6).
MyoD es uno de los marcadores más tempranos cuando se produce miogénesis. Es expresada en células satélite activadas, pero no en las quiescentes. Aunque MyoD es un marcador de mioblastomas, el desarrollo del músculo no se ve drásticamente comprometido en ratones knockout que no poseen este gen. Esto se debe probablemente a la redundancia funcional de Myf5.
Contenido
Función
La función de MyoD en el desarrollo es destinar células del mesodermo para diferenciarse en una línea de células esqueléticas, y entonces regular todo el proceso. MyoD también podría jugar un papel en la regulación de la reparación muscular. Los niveles de ARNm del gen que expresa MyoD también parecen mostrar niveles elevados en músculo esquelético envejecido.
Una de las principales acciones de MyoD es evitar que las células continúen el ciclo celular potenciando la transcripción de p21. Esto parece producirse en virtud de la homología de secuencia con c-Myc. MyoD es inhibida por las quinasas dependientes de ciclinas (Cdks). A su vez, las Cdks son inhibidas por p21. Por ello, MyoD favorece su propia actividad en la célula.
Interacciones
La proteína MyoD ha demostrado ser capaz de interaccionar con:
- HDAC1[2] [3]
- ID1[4] [5] [6] [7] [8] [9]
- ID2[5]
- Proteína del retinoblastoma[3] [10]
- STAT3[11]
- CSRP3[12]
- Cdk4[13] [14]
- CREBBP[15] [16]
- TCF3[17] [5]
- MOS[18]
- EP300[19] [16]
- c-Jun[20]
- Inhibidor 1C de quinasas dependientes de ciclinas[21]
- Receptor X retinoide alfa[22]
- MDFI[23]
Referencias
- ↑ «Entrez Gene: MYOD1 myogenic differentiation 1».
- ↑ Puri, P L; Iezzi S, Stiegler P, Chen T T, Schiltz R L, Muscat G E, Giordano A, Kedes L, Wang J Y, Sartorelli V (Oct. 2001). «Class I histone deacetylases sequentially interact with MyoD and pRb during skeletal myogenesis». Mol. Cell (United States) 8 (4): pp. 885–97. ISSN 1097-2765. PMID 12479798.
- ↑ a b Mal, A; Sturniolo M, Schiltz R L, Ghosh M K, Harter M L (Apr. 2001). «A role for histone deacetylase HDAC1 in modulating the transcriptional activity of MyoD: inhibition of the myogenic program». EMBO J. (England) 20 (7): pp. 1739–53. doi:. ISSN 0261-4189. PMID 11285237.
- ↑ Garkavtsev, Igor; Kozin Sergey V, Chernova Olga, Xu Lei, Winkler Frank, Brown Edward, Barnett Gene H, Jain Rakesh K (Mar. 2004). «The candidate tumour suppressor protein ING4 regulates brain tumour growth and angiogenesis». Nature (England) 428 (6980): pp. 328–32. doi:. PMID 15029197.
- ↑ a b c Langlands, K; Yin X, Anand G, Prochownik E V (Aug. 1997). «Differential interactions of Id proteins with basic-helix-loop-helix transcription factors». J. Biol. Chem. (UNITED STATES) 272 (32): pp. 19785–93. ISSN 0021-9258. PMID 9242638.
- ↑ Finkel, T; Duc J, Fearon E R, Dang C V, Tomaselli G F (Jan. 1993). «Detection and modulation in vivo of helix-loop-helix protein-protein interactions». J. Biol. Chem. (UNITED STATES) 268 (1): pp. 5–8. ISSN 0021-9258. PMID 8380166.
- ↑ Gupta, K; Anand G, Yin X, Grove L, Prochownik E V (Mar. 1998). «Mmip1: a novel leucine zipper protein that reverses the suppressive effects of Mad family members on c-myc». Oncogene (ENGLAND) 16 (9): pp. 1149–59. doi:. ISSN 0950-9232. PMID 9528857.
- ↑ McLoughlin, Patricia; Ehler Elisabeth, Carlile Graeme, Licht Jonathan D, Schäfer Beat W (Oct. 2002). «The LIM-only protein DRAL/FHL2 interacts with and is a corepressor for the promyelocytic leukemia zinc finger protein». J. Biol. Chem. (United States) 277 (40): pp. 37045–53. doi:. ISSN 0021-9258. PMID 12145280.
- ↑ Ling, Ming-Tat; Chiu Yung-Tuen, Lee Terence Kin Wah, Leung Steve Chin Lung, Fung Maggie Ka Lai, Wang Xianghong, Wong Kwong Fai, Wong Yong-Chuan (Sep. 2008). «Id-1 induces proteasome-dependent degradation of the HBX protein». J. Mol. Biol. (England) 382 (1): pp. 34–43. doi:. PMID 18674781.
- ↑ Gu, W; Schneider J W, Condorelli G, Kaushal S, Mahdavi V, Nadal-Ginard B (Feb. 1993). «Interaction of myogenic factors and the retinoblastoma protein mediates muscle cell commitment and differentiation». Cell (UNITED STATES) 72 (3): pp. 309–24. ISSN 0092-8674. PMID 8381715.
- ↑ Kataoka, Yoshihisa; Matsumura Itaru, Ezoe Sachiko, Nakata Soichi, Takigawa Eri, Sato Yusuke, Kawasaki Akira, Yokota Takashi, Nakajima Koichi, Felsani Armando, Kanakura Yuzuru (Nov. 2003). «Reciprocal inhibition between MyoD and STAT3 in the regulation of growth and differentiation of myoblasts». J. Biol. Chem. (United States) 278 (45): pp. 44178–87. doi:. ISSN 0021-9258. PMID 12947115.
- ↑ Kong, Y; Flick M J, Kudla A J, Konieczny S F (Aug. 1997). «Muscle LIM protein promotes myogenesis by enhancing the activity of MyoD». Mol. Cell. Biol. (UNITED STATES) 17 (8): pp. 4750–60. ISSN 0270-7306. PMID 9234731.
- ↑ Zhang, J M; Zhao X, Wei Q, Paterson B M (Dec. 1999). «Direct inhibition of G(1) cdk kinase activity by MyoD promotes myoblast cell cycle withdrawal and terminal differentiation». EMBO J. (ENGLAND) 18 (24): pp. 6983–93. doi:. ISSN 0261-4189. PMID 10601020.
- ↑ Zhang, J M; Wei Q, Zhao X, Paterson B M (Feb. 1999). «Coupling of the cell cycle and myogenesis through the cyclin D1-dependent interaction of MyoD with cdk4». EMBO J. (ENGLAND) 18 (4): pp. 926–33. doi:. ISSN 0261-4189. PMID 10022835.
- ↑ Polesskaya, A; Naguibneva I, Duquet A, Bengal E, Robin P, Harel-Bellan A (Aug. 2001). «Interaction between acetylated MyoD and the bromodomain of CBP and/or p300». Mol. Cell. Biol. (United States) 21 (16): pp. 5312–20. doi:. ISSN 0270-7306. PMID 11463815.
- ↑ a b Sartorelli, V; Huang J, Hamamori Y, Kedes L (Feb. 1997). «Molecular mechanisms of myogenic coactivation by p300: direct interaction with the activation domain of MyoD and with the MADS box of MEF2C». Mol. Cell. Biol. (UNITED STATES) 17 (2): pp. 1010–26. ISSN 0270-7306. PMID 9001254.
- ↑ Maleki, S J; Royer C A, Hurlburt B K (Jun. 1997). «MyoD-E12 heterodimers and MyoD-MyoD homodimers are equally stable». Biochemistry (UNITED STATES) 36 (22): pp. 6762–7. doi:. ISSN 0006-2960. PMID 9184158.
- ↑ Lenormand, J L; Benayoun B, Guillier M, Vandromme M, Leibovitch M P, Leibovitch S A (Feb. 1997). «Mos activates myogenic differentiation by promoting heterodimerization of MyoD and E12 proteins». Mol. Cell. Biol. (UNITED STATES) 17 (2): pp. 584–93. ISSN 0270-7306. PMID 9001211.
- ↑ Lau, P; Bailey P, Dowhan D H, Muscat G E (Jan. 1999). «Exogenous expression of a dominant negative RORalpha1 vector in muscle cells impairs differentiation: RORalpha1 directly interacts with p300 and myoD». Nucleic Acids Res. (ENGLAND) 27 (2): pp. 411–20. ISSN 0305-1048. PMID 9862959.
- ↑ Bengal, E; Ransone L, Scharfmann R, Dwarki V J, Tapscott S J, Weintraub H, Verma I M (Feb. 1992). «Functional antagonism between c-Jun and MyoD proteins: a direct physical association». Cell (UNITED STATES) 68 (3): pp. 507–19. ISSN 0092-8674. PMID 1310896.
- ↑ Reynaud, E G; Leibovitch M P, Tintignac L A, Pelpel K, Guillier M, Leibovitch S A (Jun. 2000). «Stabilization of MyoD by direct binding to p57(Kip2)». J. Biol. Chem. (UNITED STATES) 275 (25): pp. 18767–76. doi:. ISSN 0021-9258. PMID 10764802.
- ↑ Froeschlé, A; Alric S, Kitzmann M, Carnac G, Auradé F, Rochette-Egly C, Bonnieu A (Jul. 1998). «Retinoic acid receptors and muscle b-HLH proteins: partners in retinoid-induced myogenesis». Oncogene (ENGLAND) 16 (26): pp. 3369–78. doi:. ISSN 0950-9232. PMID 9692544.
- ↑ Chen, C M; Kraut N, Groudine M, Weintraub H (Sep. 1996). «I-mf, a novel myogenic repressor, interacts with members of the MyoD family». Cell (UNITED STATES) 86 (5): pp. 731–41. ISSN 0092-8674. PMID 8797820.
Enlaces externos
Categorías:- Genes del cromosoma 11
- Proteínas humanas
- Factores de transcripción
Wikimedia foundation. 2010.
